Organická analýza - Příprava vzorků k analýze – extrakční techniky

Foto: 2 Theta: Organická analýza
2 ODBĚR A PŘÍPRAVA VZORKŮ K ANALÝZE - EXTRAKČNÍ TECHNIKY, PASIVNÍ VZORKOVÁNÍ ORGANICKÝCH POLUTANTŮ
2.3 Příprava vzorků k analýze - extrakční techniky
- 2.3.1 Klasické extrakční techniky
- 2.3.1.1 Extrakce kapalina-kapalina
- 2.3.1.2 Extrakce v Soxhletově extraktoru
- 2.3.1.3 Automatizovaná Soxhletova extrakce
- 2.3.1.4 Extrakce tuhou fází
- 2.3.2 Mikroextrakční techniky
- 2.3.2.1 Mikroextrakce tuhou fází
- 2.3.2.2 Sorpční extrakce na míchadle a sorpční extrakce v headspace prostoru
- 2.3.2.3 Mikroextrakce tuhou fází s využitím stříkačky
- 2.3.2.4 Mikroextrakce jednou kapkou
- 2.3.2.5 Disperzní kapalinová mikroextrakce
- 2.3.2.6 Mikroextrakce využívající duté vlákno
- 2.3.3 Headspace extrakce – extrakce z plynné fáze
- 2.3.3.1 Statistická headspace extrakce
- 2.3.3.2 Dynamická headspace extrakce
- 2.3.4 Extrakce založené na použití alternativních rozpouštědel
- 2.3.4.1 Iontové kapaliny
- 2.3.4.2 Extrakce nadkritickou tekutinou
- 2.3.4.3 Vysokotlaká extrakce horkou vodou
- 2.3.5 Asistované extrakce
- 2.3.5.1 Extrakce mikrovlnným zářením
- 2.3.5.2 Ultrazvukové extrakce
- 2.3.5.3 Vysokotlaká extrakce rozpouštědlem
Kniha obsahuje přehled metod analýzy organických látek: Analytikům prohloubí jejich znalosti používaných metod a vedoucím pracovníkům poskytne podklady pro řešení úkolů jejich laboratoře. Je určena také pro studenty a vyučující univerzit a vědecké pracovníky.
💡 Kompletní obsah naleznete v odborné publikaci Organická analýza, kterou můžete zakoupit přímo u vydavatele 2 THETA, prostřednictvím LabRulez nebo v mnoha knihkupectvích.
Příprava vzorků k analýze – extrakční techniky
Příprava vzorku se považuje za důležitou součást analytického procesu založeného na chromatografické separaci, identifikaci a kvantitativního stanovení širokého spektra analytů, zejména ve vzorcích vyznačujících se komplexním složením matrice. Majors uvádí, že cca 61 % celkového času při analytických metodách je věnováno přípravě vzorku a cca 30 % chyb vyskytujících se v analytickém procesu souvisí s přípravou vzorku.
Příprava a zpracování vzorku je považována za potenciálně nejvíce znečišťující krok celého analytického procesu vzhledem k tomu, že se obvykle vyžaduje použití organických rozpouštědel. Příprava vzorku může zahrnovat několik kroků jako např. extrakci, mineralizaci, filtraci, destilaci a některé další operace. Pokud je to možné, je žádoucí několikakrokovou přípravu vzorku nahradit přímou analytickou metodou (analyty se stanovují přímo v původním vzorku, bez izolace a zakoncentrování). Hlavním úskalím přímých technik je, že jsou aplikovatelné pouze na vzorky s relativně čistými matricemi.
V mnoha případech, je však nutná izolace a zakoncentrování analytů. Použití tradičních extrakcí rozpouštědlem pro zkoncentrování analytů může způsobit významné znečištění životního prostředí. Proto byly vyvinuty některé „zelené“ extrakční techniky. Obecně platí, že tyto extrakční techniky vyžadují mnohem menší množství rozpouštědel a v některých případech se používají techniky, které vůbec nevyžadují přítomnost rozpouštědla v celém extrakčním procesu.
Existuje mnoho přístupů vedoucích k „zelené“ přípravě vzorků, tyto přístupy lze rozdělit do několika bodů:
- eliminace (nebo alespoň redukce) množství rozpouštědel a reagencií použitých při přípravě vzorku,
- miniaturizace přístrojů, zařízení a redukce počtu analytických operací,
- integrace různých postupů a automatizace/robotizace v přípravě vzorku,
- řádné utěsnění všech nádob používaných při přípravě vzorku,
- obnova rozpouštědel a opětovné použití,
- použití „zelených“ médií (iontové kapaliny, nadkritické tekutiny nebo přehřátá voda),
- použití faktorů ovlivňující efektivitu přípravy vzorku (zvýšená teplota, zvýšený tlak, mikrovlnná, popř. ultrazvukové energie).
Klasické extrakční techniky
EXTRAKCE KAPALINA-KAPALINA
Extrakce kapalina-kapalina (LLE) je jednou z nejstarších pre-chromatografických technik přípravy vzorku zahrnujících extrakci analytů. Tato technika je časově náročná, složitá k automatizaci, vyžaduje velkou spotřebu organických rozpouštědel a často je také doprovázena tvorbou emulzí. Organická rozpouštědla jsou toxická, těkavá a drahá. LLE jsou stále používány v analytické praxi, což je velmi často i podpořeno tím, že některá stanovení jsou stále doporučována EPA metodami a v České republice Českými státními normami, které jsou často normami Evropskými.
Při extrakci kapalina-kapalina jsou obě fáze kapalinami. Důležitou podmínkou těchto dvou kapalných fází je vzájemná nemísitelnost (v laboratorní praxi bývá jedním rozpouštědlem voda (popř. vodný roztok), zatímco druhé rozpouštědlo je organické). Extrakce z kapaliny do kapaliny je založena na přechodu rozpuštěné látky z jedné kapalné fáze do druhé. Může být použita buď k získání požadované látky z roztoku, nebo k odstranění nečistot z matrice. Pokud nalezneme vhodné extrakční činidlo, je extrakce velmi účinnou separační metodou.
EXTRAKCE V SOXHLETOVĚ EXTRAKTORU
Tato technika je využívána pro extrakci látek z tuhých matric. Jedná se o extrakci typu tuhá látka – kapalina. Přestože tuto klasickou extrakční techniku v současné době nahradily modernější extrakční techniky, je extrakce v Soxhletově extraktoru dodnes využívána jako srovnávací metoda pro jiné extrakční techniky.
Soxhletův extraktor (viz obr.) se skládá ze třech hlavních částí:
a) Baňka s kulatým dnem
b) Soxhletův nástavec
c) Chladič
 2 THETA: Schéma Soxhletova extraktoru
2 THETA: Schéma Soxhletova extraktoru
AUTOMATIZOVANÁ SOXHLETOVA EXTRAKCE
Mezi nově vzniklé a odvozené metody od klasické Soxhletovy extrakce se řadí automatizovaná Soxhletova extrakce tzv. Soxtec (obr. níže). Od roku 1994 je tato metoda schválena EPA jako standardní metoda. Tato metoda je rychlejší než klasická Soxhletova extrakce, protože kontakt mezi vzorkem a rozpouštědlem je v první fázi mnohem důraznější a rychlejší a dochází k rychlejšímu přenosu hmoty.
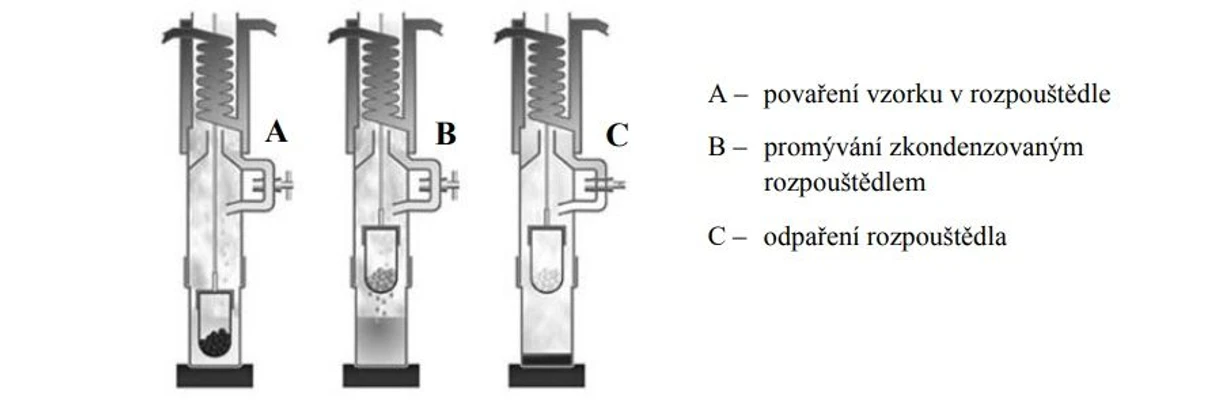 2 THETA: Schéma systému Soxtec
2 THETA: Schéma systému Soxtec
EXTRAKCE TUHOU FÁZÍ
Extrakce tuhou fází (SPE) je pravděpodobně v současné době nejčastěji využívanou extrakční technikou – ve všech jejich možných módech a formátech – analyty jsou izolovány ze složitých matric, přičemž izolace, přečištění a zakoncentrování analytu bývá dosaženo v jednom kroku. Zavedením této extrakce byly odstraněny hlavní nevýhody extrakce kapalina-kapalina (velká spotřeba organických rozpouštědel, tvorba emulzí s vodnými vzorky, nemožnost automatizace, cena, čas). Mezi hlavní výhody této extrakce oproti konvenčním metodám patří vyšší výtěžnost, účinnější zakoncentrování, nižší spotřeba organických rozpouštědel, nedochází k tvorbě emulzí, zkrácení přípravy vzorku snadná proveditelnost a možnost automatizace.
Mikroextrakční techniky
Zvyšující se poptávka po analytických metodách, které budou rychlejší, cenově výhodnější a šetrnější k životnímu prostředí byla hlavním podnětem pro zlepšení klasických postupů (LLE, aj.) používaných pro úpravu vzorku. Ve většině klasických postupů se využívá rychlá a výkonná přístrojová technika při závěrečné separaci a detekci analytů, což je ve velkém kontrastu s časově náročnými a velmi často manuálními metodami používanými pro přípravu vzorků, které velmi zpomalují celkový analytický proces. Úsilí v této oblasti v posledních desetiletích vedlo k přizpůsobení stávajících metod a vývoji nových technologií pro úsporu času, chemikálií a zlepšení celkové výkonnosti.
Mikroextrakční techniky mohou být děleny následovně:
a) Mikroextrakční techniky využívající sorbent
- Mikroextrakce tuhou fází,
- Sorpční extrakce na míchadle z kapaliny a z rovnovážné plynné fáze (headspace),
- Mikroextrakce tuhou fází s využitým stříkačky, popř. špičky pipety.
b) Mikroextrakční techniky využívající rozpouštědlo
- Mikroextrakce jednou kapkou,
- Disperzní kapalinová mikroextrakce,
- Mikroextrakce využívající duté vlákno.
MIKROEXTRAKCE TUHOU FÁZÍ
Mikroextrakce tuhou fází (SPME) je založena na rovnovážná extrakci sledovaných látek ze vzorku malým množstvím stacionární fáze umístěné na povrchu tenkého křemenného vlákna (viz obr.níže). Tato metoda se stala populární pro odběr vzorků a jako prekoncentrační technika od jejího uvedení Pawliszynem a jeho spolupracovníky. Ve srovnání s konvenčními extrakčními technikami, SPME dosáhla širokého využití zejména díky své vysoké citlivosti a jednoduchosti, která je zvýrazněna tím, že odběr vzorku a příprava vzorku jsou sloučeny do jednoho kroku a zároveň nevyžaduje použití organických rozpouštědel. Jednoduchý design SPME vlákna umožňuje rychlé a cenově efektivní extrakce a následně mohou být analyty snadno dávkovány do chromatografického systému. Různé typy vláken pokryté různými sorbenty jsou komerčně dodávány na trh od roku 1993. Většina aplikací je limitována právě vlastnostmi komerčně dodávaných vláken. Proto se snaží vědci po celém světě modifikovat tuto metodu extrakce použitím nových sorbentů jako např. iontové kapaliny, molekulárně vtištěné polymery, sol-gely, hybridní sorbenty.
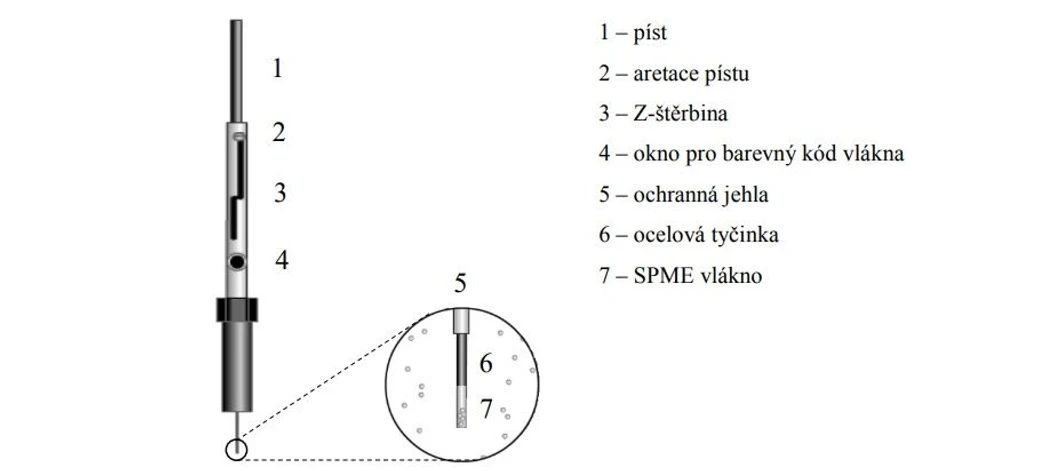 2 THETA: Schématické zobrazení zařízení používaného při SPME
2 THETA: Schématické zobrazení zařízení používaného při SPME
Desorpce analytů z vlákna může probíhat dvěma způsoby:
a) Desorpce teplem
b) Desorpce rozpouštědlem
SORPČNÍ EXTRAKCE NA MÍCHADLE Z KAPALINY A ROVNOVÁŽNÉ PLYNNÉ FÁZE
Tato extrakce byla poprvé představena v roce 1999 jako bezrozpouštědlová technika pro izolaci a obohacení organických sloučenin z vodných matric. Základní principy extrakce jsou totožné s principy SPME. Metoda je založena na sorpční extrakci, kdy analyty jsou extrahovány do vrstvy polymeru, který je nanesen na magnetickém míchadle. Rozlišujeme následující možnosti extrakce:
- míchadlo ponořené přímo v kapalném roztoku – sorpční extrakce na míchadle (SBSE),
- míchadlo je v prostoru nad vzorkem – headspace sorpční extrakce (HSSE).
Následné uvolnění analytů z polymeru může být provedeno:
- termální desorpcí v plynovém chromatografu,
- desorpcí organickým rozpouštědlem (methanol, acetonitril (100–200 µl))
MIKROEXTRAKCE TUHOU FÁZÍ S VYUŽITÍM STŘÍKAČKY
Mikroextrakce tuhou fází s využitím stříkačky (MEPS) je ve své podstatě miniaturizovaná extrakce tuhou fází a byla vynalezena a představena v laboratořích AstraZeneca ve Švédsku v roce 2004.
Při metodě MEPS je malé množství sorbentu (cca 1–2 mg) vloženo a utěsněno přímo do stříkačky (100–250 μl), do které je následně nasát vzorek, nebo mezi stříkačku a jehlu. Ke kontaktu vzorku se sorbentem dochází ve skutečnosti hned dvakrát, a to poprvé při nasátí vzorku do stříkačky a podruhé při jeho vytlačení ze stříkačky ven. Zachycené sloučeniny jsou následně vymyty vhodným rozpouštědlem přímo do nástřikového prostoru obvykle kapalinového chromatografu.
Mezi nejčastěji využívané sorbenty patří silikagel s chemicky vázanými nepolárními modifikátory, kationtově výměnný sorbent, materiály s omezeným přístupem (RAM), uhlík, polystyren-divinylbenzenový kopolymer nebo molekulárně vtištěné polymery.
MIKROEXTRAKCE JEDNOU KAPKOU
Mikroextrakce jednou kapkou (SDME) byla poprvé představena v roce 1996 jako prekoncentrační technika založená na použití mikrokapky (1,3 µl) extrakčního rozpouštědla pro extrakci dodecylsulfátu sodného. V témže roce Jeannot a Cantwell použili jako extrakční fázi kapku (8 µl) n-oktanu zavěšenou na teflonové tyčince ponořené do míchaného vodného vzorku. Po extrakci byla teflonová tyčinka vyjmuta z roztoku a extrakční organická fáze (1 µl) byla mikrostříkačkou nadávkována do plynového chromatografu. Později byla tato technika zjednodušena tak, že teflonová trubička byla nahrazena přímo hrotem mikrostříkačky. V současné době se pro extrakci využívá kapka většinou organického rozpouštědla o objemu 1–10 µl, která je zavěšena na hrotu mikrostříkačky (viz Obr.). Sledované sloučeniny jsou při dané teplotě, po určitou dobu extrahovány do kapky, která je po skončení extrakce vtažena zpět do mikrostříkačky a extrakt je následně analyzován vhodnou analytickou metodou, a to bez potřeby zařazení desorpčního kroku. Hlavní výhodou SDME je to, že pro každou extrakci je vždy používána nová extrakční fáze.
Principiálně lze SDME provést v následujících módech:
a) Přímé vzorkování z roztoku (DI-SDME)
b) Vzorkování z prostoru nad vzorkem (HS-SDME)
c) Průtoková mikroextrakce (CFME)
 2 THETA: Uspořádání metody SDME v headspace modifikaci
2 THETA: Uspořádání metody SDME v headspace modifikaci
DISPERZNÍ KAPALINOVÁ MKROEXTRAKCE
Disperzní kapalinová mikroextrakce (DLLME) odvozena od LLE extrakce. Tato metoda je rychlou a jednoduchou metodou extrakce organických látek z vodných vzorků. Při extrakci je směs extrakčního (nízká rozpustnost ve vodě, vyšší hustota než voda, schopnost extrahovat dané analyty – často halogenované uhlovodíky jako např. chloroform, tetrachlorethylen) a dispergujícího rozpouštědla (mísitelné s vodou a extrakční fází – např. acetonitril, methanol, aceton) prudce vstříknuta do vodného vzorku, a dochází k tvorbě velmi jemných kapiček extrakčního rozpouštědla, které jsou rozptýleny v roztoku vzorku. Při extrakci dochází k interakci analytů s extrakčním rozpouštědlem, přičemž plocha fázového rozhraní mezi vzorkem a rozpouštědlem je díky tvorbě jemných kapiček velká. Po extrakci je směs centrifugována, dochází k sedimentaci extraktu na kónické dno vzorkovací nádoby a extrakt je pak analyzován vhodnou instrumentální technikou. Mezi hlavní výhody metody DLLME patří především jednoduchost, rychlost, nízké náklady, vysoká výtěžnost a velké hodnoty obohacovacího faktoru. DLLME je kompatibilní s HPLC i GC.
MIKROEXTRAKCE VYUŽÍVAJÍCÍ DUTÉ VLÁKNO
Mikroextrakci využívající duté vlákno naplněné vhodnou sorpční vrstvou (HF-LPME) vyvinuli v roce 1997 He a Lee proto, aby odstranili nežádoucí křehkost mikrokapky při SDME. Při této metodě jsou sledované sloučeniny ze vzorku (donorová fáze) extrahovány do organické fáze s vodou nemísitelného rozpouštědla imobilizovaného v pórech dutého vlákna. Při extrakci je pH vzorku voleno tak, aby byla co nejvíce potlačena ionizace extrahovaných látek, čímž se snižuje jejich rozpustnost ve vodě. Na konci procesu jsou sledované sloučeniny reextrahovány do vhodného rozpouštědla uvnitř dutého vlákna (akceptorová fáze). Mezi hlavní výhody HF-LPME patří především to, že extrakční kapalina je mechanicky chráněna a je tak zabráněno jejímu pronikání do vzorku během extrakčního procesu. Metodu HF-LPME je možné realizovat ve dvoufázovém nebo třífázovém systému (Obr.).
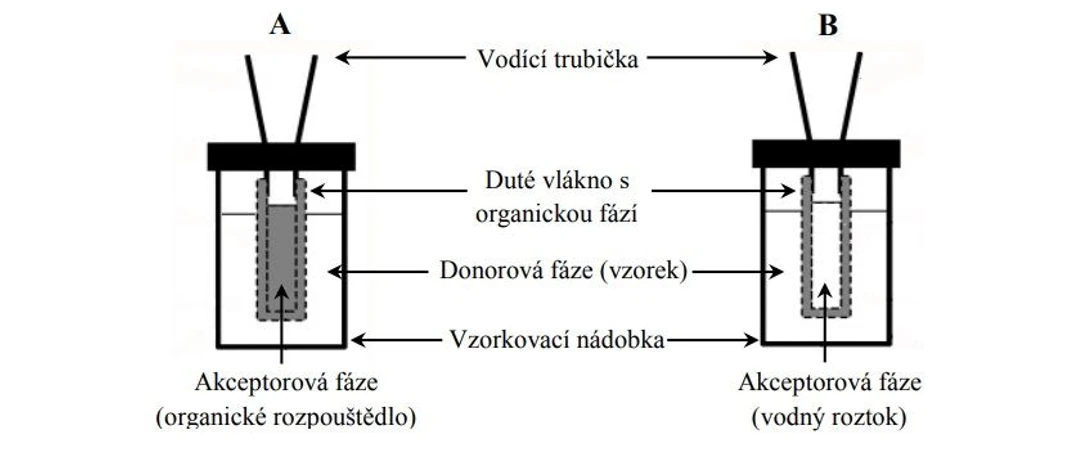 2 THETA: Uspořádání při HF LPME. A – dvoufázový systém, B – třífázový systém)
2 THETA: Uspořádání při HF LPME. A – dvoufázový systém, B – třífázový systém)
Headspace extrakce – extrakce z plynné fáze
Jedna z nejčastěji využívaných technik pro izolaci těkavých organických látek z kapalných a tuhých vzorků je extrakce z plynné fáze nad vzorkem – headspace. Technika headspace je založena na uvolňování těkavých analytů z matrice, která může být tuhá nebo kapalná. Efektivní uvolnění z matrice je možné pro těkavé, polotěkavé, nepolární a slabě polární sloučeniny. Tato metoda je rychlá, eliminuje negativní vliv sloučenin obsažených v matrici, které mohou ztěžovat analýzu a kontaminovat chromatografický systém.
Tato technika je zcela bezrozpouštědlová a rozlišujeme dva základní typy:
- statická headspace extrakce,
- dynamická headspace extrakce neboli „purge and trap“.
STATICKÁ HEADSPACE EXTRAKCE
Statická headspace extrakce bývá také označovaná jako rovnovážná headspace extrakce nebo pouze headspace. Je jednou z nejčastějších technik pro kvalitativní a kvantitativní analýzu těkavých organických sloučenin z tuhých nebo kapalných matric. Dochází neustále k ustavování rovnováhy mezi vzorkem (ať tuhým nebo kapalným) a plynnou fází nad ním. Následně je plynná fáze analyzována společně s těkavými sloučeninami uvolněnými ze vzorku.
Analytický proces se skládá ze dvou částí:
- ustavení rovnováhy mezi analyzovaným vzorkem umístěným ve vhodné plynotěsné nádobce nejčastěji o objemu 10–20 ml a plynnou fází,
- následně je plynná fáze nad vzorkem manuálně nebo automaticky plynotěsnou stříkačkou nadávkována do chromatografického systému a analyzována.
Tato extrakce je základním nástrojem pro analýzu těkavých organických sloučenin zejména při analýze prostředí, analýze chutí a vůní, analýze léčiv a farmaceutických produktů a při analýze klinických a biologických vzorků. Vzhledem k limitované citlivosti je tato metoda využívána zejména pro využití v koncentračních úrovních ppb až jednotek procent.
DYNAMICKÁ HEADSPACE EXTRAKCE
Roztokem vzorku (nebo plynnou fází nad vzorkem) prochází plyn (čištěný nebo syntetický vzduch, dusík, helium nebo argon), který unáší těkavé organické látky, které jsou následně zachytávány na sorbentu. V tomto případě nejsou těkavé analyty v rovnováze s plynnou fází a matricí. Místo toho jsou kontinuálně odstraňovány procházejícím plynem. Velikost nádobek používaných pro tuto extrakci je 5 a 25 ml. Po zachycení na sorbentu jsou zakoncentrované analyty uvolněny desorpcí do plynového chromatografu. Tato metoda je vhodná pro tuhé i kapalné vzorky obsahující těkavé organické látky stopové koncentrační úrovně (ppt–ppb).
Extrakce založené na použití alternativních rozpouštědel
Rozpouštědla jsou široce používaná v analytických laboratořích a průmyslu. Přes všechna preventivní opatření, tato rozpouštědla znečišťují životní prostředí, protože je obtížné je recyklovat. Vědečtí pracovníci se proto zaměřují na snížení spotřeby rozpouštědel prostřednictvím rozvoje bezrozpouštědlových procesů a účinnějších recyklací. Tyto přístupy mají svá omezení, což vyžaduje předcházení znečištění a hledání ekologicky nezávadných alternativních rozpouštědel. V průběhu posledních 15 let nová, nekonvenční alternativní rozpouštědla, přilákala velkou pozornost jak z akademické sféry, tak z průmyslu. Mezi takováto rozpouštědla patří iontové kapaliny, nadkritické tekutiny jako oxid uhličitý, podkritická stlačená voda a fluorové fáze.
IONTOVÉ KAPALINY
Jak zmiňují Joshi a Anderson ve své publikaci, historie iontových kapalin začala před více než sto lety. Uvádějí, že první zmínka o iontových kapalinách se nachází v článku Gabriela a Weinera z roku 1888 (bod tání připravené iontové kapaliny byl v rozmezí 52–55 °C). V roce 1914 Paul Walden v Petrohradě připravil první iontovou kapalinu – ethylamonium nitrát, s teplotou tání 17 °C.
Jako iontové kapaliny (ILs) jsou označovány takové látky, které sestávají z organického kationtu a anorganického nebo i organického aniontu a mají bod tání nižší než 100 °C. V současnosti jsou středem zájmu zejména takové iontové kapaliny, které jsou kapalné již při laboratorní teplotě, tyto iontové kapaliny s teplotou tání pod laboratorní teplotou (25 °C) jsou označovány zkratkou RTILs.
Tyto kapaliny jsou šetrné k životnímu prostředí a jsou označovány jako alternativní rozpouštědla ke konvenčním rozpouštědlům a v publikacích jsou označovány jako „zelená rozpouštědla“. RTILs mohou mít vlastnosti hydrofilní nebo hydrofobní, záleží na struktuře kationtu a aniontu.
EXTRAKCE NADKRITICKOU TEKUTINOU
Extrakce nadkritickou tekutinou byla zavedena do laboratorní praxe K. Zoselem v roce 1978. Od té doby roste zájem o tuto analytickou techniku, která je relativně rychlá a k extrakci používá nejčastěji CO₂, který je netoxický, chemicky stabilní, inertní, nehořlavý, cenově dostupný a šetrný k životnímu prostředí. Mezi jeho hlavní výhody patří snadné dosažení kritické teploty (Tk = 31,1 °C) a kritického tlaku (pk = 7,38 MPa). Mezi hlavní nevýhodu nejčastěji používané nadkritické tekutiny CO₂ v praxi patří její nepolární charakter. Selektivní extrakce různých skupin analytů však může být dosaženo zvýšením extrakční síly nadkritických tekutin za použití různých modifikátorů a optimalizací dané extrakce. Porovnání kritických parametrů rozpouštědel rovněž použitelných pro SFE je uvedeno v tabulce.
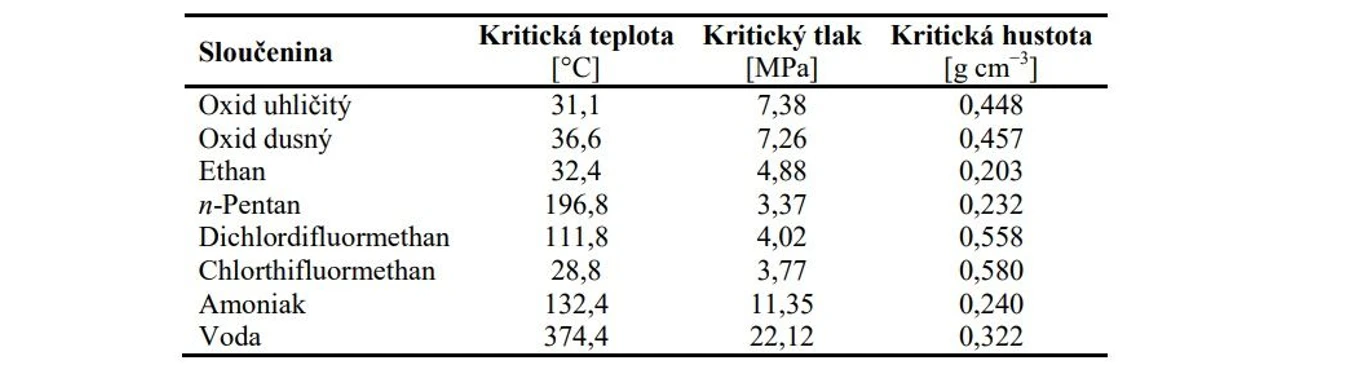 2 THETA: Kritické podmínky pro vybraná rozpouštědla používaná při SFE
2 THETA: Kritické podmínky pro vybraná rozpouštědla používaná při SFE
Vzhledem k tomu, že CO₂ je za normálních podmínek plyn, dojde po skončení extrakce k jeho vytěkání do atmosféry. Je tedy třeba vyextrahované složky kvantitativně zachytit. Existuje několik metod používaných pro záchyt extrahovaných analytů:
a) Do organického rozpouštědla
b) Na tuhý sorbent
c) Na inertní materiál
d) Do přehřátých par rozpouštědla
e) On-line záchyt
VYSOKOTLAKÁ EXTRAKCE HORKOU VODOU
Pro extrakci horkou vodou za vysokého tlaku je v literatuře uváděno několik zkratek – PHWE (pressurized hot water extraction), SWE (subcritical water extraction) a PLPW (pressurized low polarity water extraction). Při této extrakci se používají teploty v rozmezí od bodu varu rozpouštědla (100 °C) do kritické teploty vody (374 °C), zatímco pracovní tlak je udržován v rozmezí 3,5–20 MPa tak, aby voda zůstala v kapalné fázi při celém extrakčním procesu. Při těchto podmínkách (tlaku a teplotě) se fyzikální a chemické vlastnosti vody dramaticky mění.
Mezi hlavní parametry ovlivňující extrakci patří:
- teplota extrakce (je hlavním faktorem, který ovlivňuje účinnost extrakce a selektivitu),
- doba extrakce a tlak,
- přídavek organického rozpouštědla nebo povrchově aktivní látky,
- průtoková rychlost vody (v případě dynamické extrakce).
Se vzrůstající teplotou vody dochází k:
- usnadnění difúze analytu (vodivost vody při 25 °C je asi desetkrát nižší než u vody při 200 °C),
- usnadnění přenosu hmoty narušením mezimolekulárních sil (např. van der Waalsovy síly, vodíkové vazby),
- snížení viskozity vody (umožňující lepší penetraci matricových částic),
- snížení povrchového napětí (umožňuje lépe smáčet matrici vzorku).
Asistované extrakce
EXTRAKCE MIKROVLNNÝM ZÁŘENÍM
Mikrovlnná extrakce našla uplatnění převážně v environmentální chemii a v poslední době se také hojně využívá při extrakci látek z biologických matric. Mezi parametry, které lze optimalizovat při vývoji MAE extrakce patří: typ rozpouštědla, matrice (velikost částic, původ), čas, teplota a mikrovlnná síla (uváděná ve Wattech). Hlavní výhodou MAE je krátká doba extrakce. Tato doba je závislá převážně na typu zvoleného rozpouštědla a na teplotě. MAE je proces používající mikrovln k ohřátí rozpouštědla nebo vzorku a k převedení
požadovaných sloučenin z matrice do rozpouštědla.
Existují dvě možnosti provedení této extrakce:
a) V uzavřeném systému (za zvýšeného tlaku)
b) V otevřeném systému (za atmosférického tlaku)
ULTRAZVUKOVÉ EXTRAKCE
Ultrazvuk spadá do oblasti akustiky a náleží mu celý frekvenční rozsah nad slyšitelností lidského ucha. V ultrazvukové technice je stanovena tato hranice nad 20 kHz. Účinky ultrazvuku při šíření v daném prostředí závisí na intenzitě (amplitudě), frekvenci kmitů a na vlastnostech prostředí. Působením ultrazvukové vibrace dochází k zajištění dokonalého kontaktu mezi vzorkem a rozpouštědlem. Ultrazvuková energie působí několika způsoby. Vysoká teplota zvyšuje rozpustnost a difuzivitu látek a vysoké tlaky zvyšují penetrační sílu rozpouštědla do tuhé nebo kapalné fáze. Oba účinky mají za následek lepší výtěžnost analytů a zkrácení doby extrakce. Důležitým a neopomenutelným jevem je kavitace, což je fyzikální jev v kapalině, při kterém vznikají, vyvíjejí se a zanikají kavitační bubliny (průměr řádově v µm). Kavitace vzniká v proudících kapalinách nebo při pohlcení ultrazvukových vln v kapalině v místech, kde dochází k náhlým tlakovým změnám.
Pro ultrazvukovou extrakci můžeme použít dva základní typy zařízení: (Obr.)
- ultrazvukovou sondu
- ultrazvukovou lázeň
 2 THETA: Příklady instrumentace pro ultrazvukové extrakce. A - ultrazvuková lázeň, B – ultrazvuková sonda
2 THETA: Příklady instrumentace pro ultrazvukové extrakce. A - ultrazvuková lázeň, B – ultrazvuková sonda
V případě ultrazvukových lázní bývá vysílač ultrazvukových vln obvykle umístěn ve středu ultrazvukové lázně, přičemž kavitační energie uvnitř lázně má proměnlivou intenzitu. V tomto případě dochází ke ztrátám ultrazvukové energie působící na vzorek, což může být způsobeno materiálem a tloušťkou stěny nádobky se vzorkem.
VYSOKOTLAKÁ EXTRAKCE ROZPOUŠTĚDLEM
Tato extrakce bývá v anglických publikacích označována různými zkratkami jako např.
- PLE (Pressurized Liquid Extraction),
- ASE (Accelerated Solvent Extraction),
- PFE (Pressurized Fluid Extraction),
- PHSE (Pressurized Hot Solvent Extraction).
Jedná se o techniku využívající pro extrakci analytů rozpouštědla při teplotách nad atmosférickým bodem varu, a která jsou vlivem vyššího pracovního tlaku udržována v kapalném stavu. Používané teploty a tlaky jsou však vždy pod příslušnými kritickými hodnotami. Tato extrakce byla poprvé popsána v roce 1995 Richterem a jeho spolupracovníky. Je to metoda vysoce účinná pro extrakci z tuhých a polotuhých matric. Je založena na principu extrakce v systému tuhá látka – kapalina. Extrakčním mediem může být jakékoli polární i nepolární rozpouštědlo, případně směs rozpouštědel. Zvýšením teploty se viskozita a povrchové napětí sníží a zvýší se rychlost difuze, rozpustnost a přenos hmoty. Tyto změny zlepšují kontakt analytu s rozpouštědlem a tím zvyšují výtěžek extrakce. Rozpouštědlo je zahřáto nad atmosférický bod varu a zvýšeným tlakem je udržováno v kapalném stavu.
- [1] M. Abdel-Rehim, Journal of Chromatography A 1217 (2010) 2569.
- [2] M. Abdel-Rehim, Journal of Chromatography B 801 (2004) 317.
- [3] M. Abdel-Rehim, Z. Altun, L. Blomberg, Journal of Mass Spectrometry 39 (2004) 1488.
- [4] S.S. Al-Rawi, A.H. Ibrahim, A.S.A. Majid, A.M.S.A. Majid, M.O. Ab Kadir, Journal of Food Engineering 119 (2013) 595.
- [5] Z. Altun, M. Abdel-Rehim, L.G. Blomberg, Journal of Chromatography B 813 (2004) 129.
- [6] P.T. Anastas, Critical Reviews in Analytical Chemistry 29 (1999) 167.
- [7] J.L. Anderson, D.W. Armstrong, G.-T. Wei, Analytical Chemistry 78 (2006) 2892.
- [8] Y.H. Ardakani, M.R. Rouini, Journal of Pharmaceutical and Biomedical Analysis 44 (2007) 1168.
- [9] M. Arias, I. Penichet, F. Ysambertt, R. Bauza, M. Zougagh, A. Rios, Journal of Supercritical Fluids 50 (2009) 22.
- [10] S. Armenta, S. Garrigues, M. de la Guardia, TrAC - Trends in Analytical Chemistry 27 (2008) 497.
- [11] C.L. Arthur, L.M. Killam, S. Motlagh, M. Lim, D.W. Potter, J. Pawliszyn, Environmental Science & Technology 26 (1992) 979.
- [12] C.L. Arthur, J. Pawliszyn, Analytical Chemistry 62 (1990) 2145.
- [13] M.H. Banitaba, S.S.H. Davarani, S.K. Movahed, Journal of Chromatography A 1325 (2014) 23.
- [14] G. Basaglia, J. Fiori, A. Leoni, R. Gotti, Analytical Letters 47 (2014) 268.
- [15] R. Batlle, P. Lopez, C. Nerin, C. Crescenzi, Journal of Chromatography A 1185 (2008) 155.
- [16] M.A. Bello-Lopez, M. Ramos-Payan, J.A. Ocana-Gonzalez, R. Fernandez-Torres, M. Callejon-Mochon, Analytical Letters 45 (2012) 804.
- [17] S. Bøwadt, B. Johansson, F. Pelusio, B.R. Larsen, C. Rovida, Journal of Chromatography A 662 (1994) 424.
- [18] V.M. Burin, S. Marchand, G. de Revel, M.T. Bordignon-Luiz, Talanta 117 (2013) 87.
- [19] J.L. Capelo, C. Maduro, C. Vilhena, Ultrasonics Sonochemistry 12 (2005) 225.
- [20] A. Capuzzo, M.E. Maffei, A. Occhipinti, Molecules 18 (2013) 7194.
- [21] N. Carro, I. Garcia, M. Ignacio, A. Mouteira, Analytical Letters 45 (2012) 2161.
- [22] M. Castro-Puyana, J.A. Mendiola, E. Ibañez, TrAC - Trends in Analytical Chemistry 52 (2013) 23.
- [23] T. Cecchi, B. Alfei, Food Chemistry 141 (2013) 2025.
- [24] N. De Brabanter, W. Van Gansbeke, L. Geldof, P. Van Eenoo, Biomedical Chromatography 26 (2012) 1416.
- [25] J.R. Dean, Extraction Methods for Environmental Analysis, John Wiley & Sons, Chichester, 1998.
- [26] A. Delazar, L. Nahar, S. Hamedeyazdan, S. Sarker, in S.D. Sarker, L. Nahar (Eds.), Natural Products Isolation, Humana Press, 2012.
- [27] E. Destandau, E. Lesellier, Chromatographia 68 (2008) 985.
- [28] Z. Ding, S. Peng, W. Xia, H. Zheng, X. Chen, L. Yin, International Journal of Analytical Chemistry 2014 (2014) 697260.
- [29] W. Fan, Y. Xu, Y. Han, Journal of the Institute of Brewing 117 (2011) 61.
- [30] J. Fischer, D. Brinkmann, P.W. Elsinghorst, M. Wuest, Meat Science 91 (2012) 261.
- [31] K. Ganzler, A. Salgo, K. Valko, Journal of Chromatography 371 (1986) 299.
- [32] L.M. Giner, J.V. Rodrigo, A.C.F. Navarro, V.L.C. Burillo, Energy & Fuels 10 (1996) 1005.
- [33] I. Giraldez, M. Ruiz-Montoya, M. Delgado-Rodriguez, M.J. Diaz, Journal of Residuals Science & Technology 10 (2013) 107.
- [34] T. Greibrokk, Journal of Chromatography A 703 (1995) 523.
- [35] J. Hanusek, Chemické Listy 99 (2005) 263.
- [36] K. Hartonen, S. Bøwadt, S.B. Hawthorne, M.-L. Riekkola, Journal of Chromatography A 774 (1997) 229.
- [37] Y. He, H.K. Lee, Analytical Chemistry 69 (1997) 4634.
- [38] M. Herrero, M. Castro-Puyana, J.A. Mendiola, E. Ibañez, TrAC -Trends in Analytical Chemistry 43 (2013) 67.
- [39] T.D. Ho, A.J. Canestraro, J.L. Anderson, Analytica Chimica Acta 695 (2011) 18.
- [40] T.D. Ho, H. Yu, W.T.S. Cole, J.L. Anderson, Analytical Chemistry 84 (2012) 9520.
- [41] X. Hu, Q. Zhou, Chromatographia 74 (2011) 489.
- [42] E. Ibanez, A. Kubatova, F.J. Senorans, S. Cavero, G. Reglero, S.B. Hawthorne, Journal of Agricultural and Food Chemistry 51 (2003) 375.
- [43] H.-G. Jansen, X. Lou, in A.J. Handley (Ed.), Extraction methods in organic analysis. Sheffield Academic Press, Sheffield, 1999.
- [44] M.A. Jeannot, F.F. Cantwell, Analytical Chemistry 68 (1996) 2236.
- [45] M.A. Jeannot, F.F. Cantwell, Analytical Chemistry 69 (1997) 235.
- [46] B. Jurado-Sanchez, E. Ballesteros, M. Gallego, Science of the Total Environment 463 (2013) 293.
- [47] A. Kabir, K.G. Furton, A. Malik, TrAC - Trends in Analytical Chemistry 45 (2013) 197.
- [48] H. Kataoka, TrAC - Trends in Analytical Chemistry 22 (2003) 232.
- [49] H. Kataoka, H.L. Lord, in J. Pawliszyn (Ed.), Sampling and Sample Preparation for Field and Laboratory. Elsevier Science B.V., Amsterdam, 2002.
- [50] J. King, J. France, in B. Wenclawiak (Eds), Analysis with Supercritical Fluids: Extraction and Chromatography, Springer Berlin Heidelberg, 1992.
- [51] G. Knobel, K. Calimag-Williams, A.D. Campiglia, Analytical Methods 5 (2013) 1577.
- [52] P.L. Kole, J. Millership, J.C. McElnay, Talanta 85 (2011) 1948.
- [53] D. Kou, S. Mitra, in Sample Preparation Techniques in Analytical Chemistry, John Wiley & Sons, Inc., 2003.
- [54] O. Kruger, G. Christoph, U. Kalbe, W. Berger, Talanta 85 (2011) 1428.
- [55] R. Krzyzanowski, B. Leszczynski, Toxicology Letters 164 (2006) S233.
- [56] O. Lasekan, A. Khatib, H. Juhari, P. Patiram, S. Lasekan, Food Chemistry 141 (2013) 2089.
- [57] J. Lee, H.K. Lee, K.E. Rasmussen, S. Pedersen-Bjergaard, Analytica Chimica Acta 624 (2008) 253.
- [58] H. Liu, P.K. Dasgupta, Analytical Chemistry 68 (1996) 1817.
- [59] H. Liu, H. Wang, C. Li, L. Wang, Z. Pan, L. Wang, Journal of Chromatography B 945 (2014) 53.
- [60] W.P. Liu, H.K. Lee, Analytical Chemistry 72 (2000) 4462.
- [61] M.D. Luque de Castro, F. Priego-Capote, Journal of Chromatography A 1217 (2010) 2383.
- [62] R. Maia, M. Correia, I.M. Bras Pereira, V.M. Beleza, Microchemical Journal 112 (2014) 164.
- [63] R.E. Majors, LC GC-Magazine of Separation Science 9 (1991) 16.
- [64] M.B. Mariani, V. Giannetti, E. Testani, Food Analytical Methods 7 (2014) 64.
- [65] M.B. Mariani, V. Giannetti, E. Testani, V. Ceccarelli, Journal of AOAC International 96 (2013) 1430.
- [66] A. Marrufo-Curtido, M.J. Cejudo-Bastante, E. Duran-Guerrero, R. Castro-Mejias, R. Natera-Marin, F. Chinnici, C. Garcia-Barroso, LWT-Food Science and Technology 47 (2012) 332.
- [67] A. Martín-Esteban, TrAC - Trends in Analytical Chemistry 45 (2013) 169.
- [68] A. Menezes Filho, P.N. dos Santos, P.A.d.P. Pereira, Microchemical Journal 96 (2010) 139.
- [69] J. Merib, V. Simao, A.N. Dias, E. Carasek, Journal of Chromatography A 1321 (2013) 30.
- [70] D.J. Miller, S.B. Hawthorne, M. Ellen, P. McNally, Analytical Chemistry 65 (1993) 1038.
- [71] F.S. Mirnaghi, J. Pawliszyn, Analytical Chemistry 84 (2012) 8301
- [72] R. Molín, R Přibyl, Chemické Listy 92 (1998) 784.
- [73] N. Moreira, S. Meireles, T. Brandao, P.G. de Pinho, Talanta 117 (2013) 523.
- [74] J. Möller, E. Strömberg, S. Karlsson: European Polymer Journal 44 (2008) 1583.
- [75] L.J. Mulcahey, L.T. Taylor, Analytical Chemistry 64 (1992) 2352.
- [76] A. Mustafa, C. Turner, Analytica Chimica Acta 703 (2011) 8.
- [77] M. Nilsson, M. Waldebäck, G. Liljegren, H. Kylin, K. Markides, Fresenius Journal of Analytical Chemistry 370 (2001) 913.
- [78] L. Nováková, H. Vlčková, Analytica Chimica Acta 656 (2009) 8.
- [79] E.S. Ong, J.S.H. Cheong, D. Goh, Journal of Chromatography A 1112 (2006) 92.
- [80] B. Ovalle-Magallanes, I. Rivero-Cruz, R. Mata, Pharmaceutical Biology 52 (2014) 117.
- [81] J. Pawliszyn, Solid Phase Microextraction: Theory and Practice, Wiley–VCh, New York, 1997.
- [82] M.A. Pedroza, A. Zalacain, J. Felix Lara, M. Rosario Salinas, Food Research International 43 (2010) 1003.
- [83] U. Petersson, K.E. Markides, Journal of Chromatography A 734 (1996) 311.
- [84] C. Petisca, T. Perez-Palacios, O. Pinho, I.M.P.L.V.O. Ferreira, Food Analytical Methods 7 (2014) 81.
- [85] J. Płotka, M. Tobiszewski, A.M. Sulej, M. Kupska, T. Górecki, J. Namieśnik, Journal of Chromatography A 1307 (2013) 1.
- [86] O.J. Pozo, P. Van Eenoo, W. Van Thuyne, K. Deventer, F.T. Delbeke, Journal of Chromatography A 1183 (2008) 108.
- [87] G. Purcaro, M. Picardo, L. Barp, S. Moret, L.S. Conte, Journal of Chromatography A 1307 (2013) 166.
- [88] M. Rezaee, Y. Assadi, M.R. Milani Hosseini, E. Aghaee, F. Ahmadi, S. Berijani, Journal of Chromatography A 1116 (2006) 1.
- [89] S. Reale, L. Pace, A.A. D'Archivio, F. De Angelis, G. Marcozzi, Natural Product Research 28 (2014) 61.
- [90] B.E. Richter, J.L. Ezzell, D. Felix, K.A. Roberts, D.W. Later, American Laboratory 27 (1995) 24.
- [91] B.E. Richter, B.A. Jones, J.L. Ezzell, N.L. Porter, N. Avdalovic, C. Pohl, Analytical Chemistry 68 (1996) 1033.
- [92] J. Robles-Molina, B. Gilbert-Lopez, J.F. Garcia-Reyes, A. Molina-Diaz, Talanta 117 (2013) 382.
- [93] R. Rodriguez Madrera, B. Suarez Valles, Journal of Food Science 76 (2011) C1326.
- [94] G. Roy, R. Vuillemin, J. Guyomarch, Talanta 66 (2005) 540.
- [95] B. Sgorbini, C. Cagliero, C. Cordero, E. Liberto, P. Rubiolo, M.R. Ruosi, C. Bicchi, Journal of Chromatography A 1265 (2012) 39.
- [96] Q. Shen, W. Dong, Y. Wang, L. Gong, Z. Dai, H.-Y. Cheung, Journal of Pharmaceutical and Biomedical Analysis. 80 (2013) 136.
- [97] J.J. Shu, C. Li, M.M. Liu, H.L. Liu, X.H. Feng, W.F. Tan, F. Liu, Chromatographia 75 (2012) 1421.
- [98] G.C. Slack, N.H. Snow, D. Kou, in Sample Preparation Techniques in Analytical Chemistry, John Wiley & Sons, Inc., 2003.
- [99] N.H. Snow, G.P. Bullock, Journal of Chromatography A 1217 (2010) 2726.
- [100] N.H. Snow, G.C. Slack, TrAC - Trends in Analytical Chemistry 21 (2002) 608.
- [101] H.A.L. Souza, N. Bragagnolo, Journal of Agricultural and Food Chemistry 62 (2014) 590.
- [102] E.A. Souza-Silva, V. Lopez-Avila, J. Pawliszyn, Journal of Chromatography A 1313 (2013) 139.
- [103] E.A. Souza-Silva, J. Pawliszyn, Analytical Chemistry 84 (2012) 6933.
- [104] E.A. Souza-Silva, S. Risticevic, J. Pawliszyn, TrAC - Trends in Analytical Chemistry 43 (2013) 24.
- [105] S. Sporring, S. Bowadt, B. Svensmark, E. Bjorklund, Journal of Chromatography A 1090 (2005) 1.
- [106] V. Štengl, J. Šubrt, Chemické Listy 98 (2004) 324.
- [107] B. Tang, W. Bi, M. Tian, K.H. Row, Journal of Chromatography B 904 (2012) 1.
- [108] M. Tankiewicz, C. Morrison, M. Biziuk, Talanta 107 (2013) 1.
- [109] F. Tateo, M. Bononi, Journal of Food Composition and Analysis 16 (2003) 721.
- [110] C.C. Teo, S.N. Tan, J.W.H. Yong, C.S. Hew, E.S. Ong, Journal of Chromatography A 1217 (2010) 2484.
- [111] A.L. Theis, A.J. Waldack, S.M. Hansen, M.A. Jeannot, Analytical Chemistry 73 (2001) 5651.
- [112] E.M. Thurman, S. Mills, Solid-Phase Extraction: Principles and Practice, Wiley, 1998.
- [113] C. Turner, C. Sparr Eskilsson, E. Björklund, Journal of Chromatography A 947 (2002) 1.
- [114] L. Urbánek, D. Solichová, B. Melichar, J. Dvořák, I. Svobodová, P. Solich, Analytica Chimica Acta 573–574 (2006) 267.
- [115] J. Urbanova, K. Pencikova, J. Gregorova, B. Hohnova, L. Stavikova, P. Karasek, M. Roth, E. Taborska, Phytochemical Analysis 23 (2012) 477.
- [116] J. Vejrosta, P. Karásek, J. Planeta, Analytical Chemistry 71 (1999) 905.
- [117] A.E. Visser, W.M. Reichert, R.P. Swatloski, H.D. Willauer, J.G. Huddleston, R.D. Rogers, in R.D. Rogers, K.R. Seddon (Eds.), Ionic Liquids: Industrial Applications for Green Chemistry, Amer Chemical Soc, Washington, 2002.
- [118] M. Wasielewska, B. Zygmunt, J.L. Anderson, Chromatographia 77 (2014) 151.
- [119] M.J.M. Wells, in Sample Preparation Techniques in Analytical Chemistry, John Wiley & Sons, Inc., 2003.
- [120] L. Xu, C. Basheer, H.K. Lee, Journal of Chromatography A 1152 (2007) 184.
- [121] C. Yang, J. Wang, D.H. Li, Analytica Chimica Acta 799 (2013) 8.
- [122] G.-T. Zhu, X.-M. He, X.-S. Li, S.-T. Wang, Y.-B. Luo, B.-F. Yuan, Y.-Q. Feng, Journal of Chromatography A 1316 (2013) 23.




